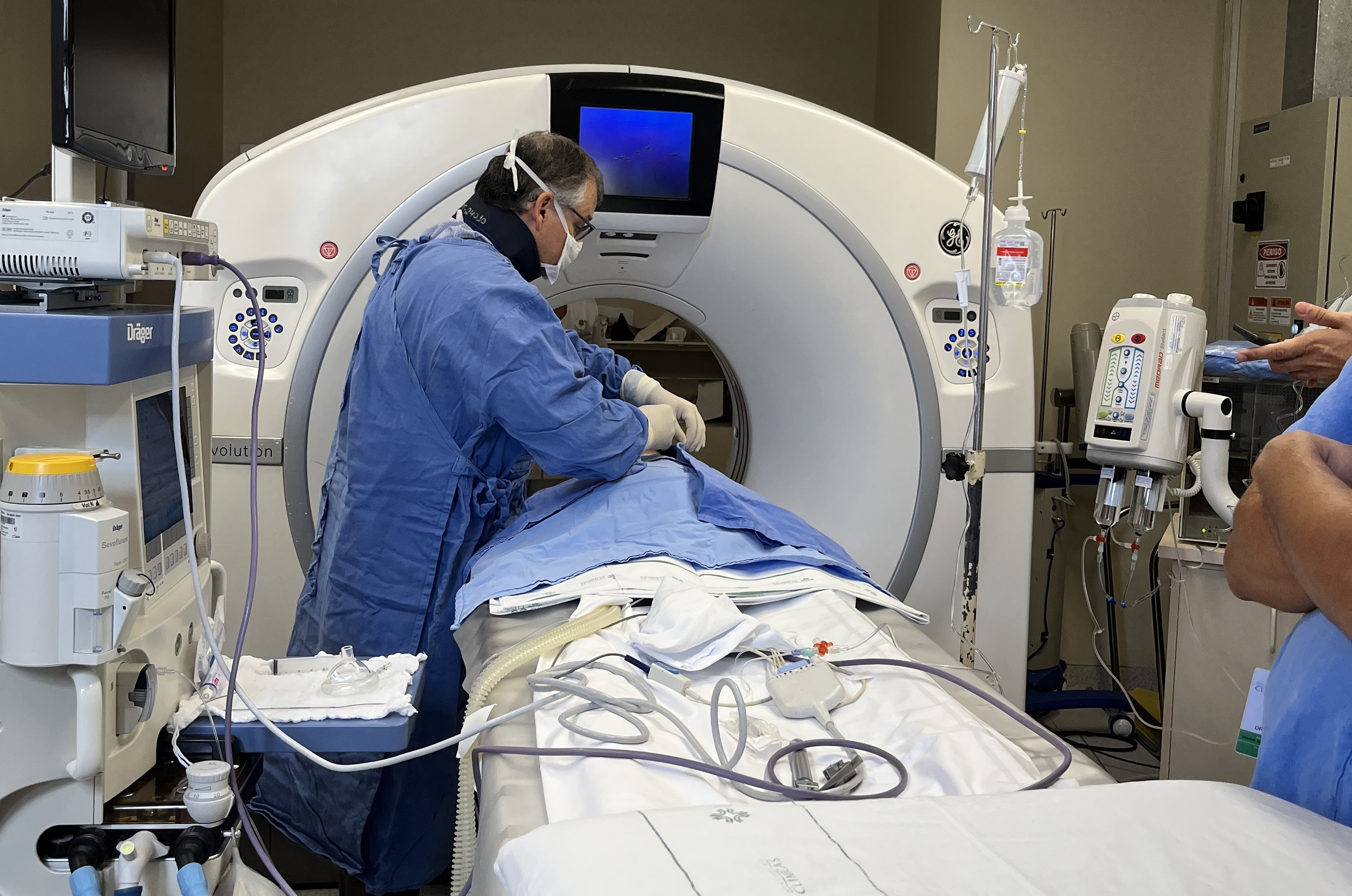
Bebê brasileiro é primeiro paciente em teste de terapia gênica contra atrofia muscular espinhal
Um bebê brasileiro de menos de um ano é o primeiro paciente da terapia de DNA desenvolvida contra atrofia muscular espinhal (AME), doença rara que causa paralisia potencialmente letal, que está sendo testada no país. O ensaio clínico desse tratamento, aprovado pela Agência Nacional de Vigilância Sanitária em novembro passado, teve início em janeiro com a infusão dos genes terapêuticos na criança, na esperança de que corrijam o defeito inato que ela carrega. Polilaminina: Grupo controle pode não receber placebo no estudo clínico? O primeiro procedimento foi realizado no Hospital de Clínicas de Porto Alegre, que fará o acompanhamento deste e de outros pacientes submetidos à terapia gênica ao longo do teste. A identidade do bebê que inaugurou o projeto foi preservada. A AME não tem cura e é causada pela mutação em um gene necessário para produzir uma proteína vital para neurônios conectados a músculos. A técnica inovadora de tratamento consiste em usar um vírus de DNA modificado que insere no paciente a versão corrigida do gene. Psicodélicos: Ayahuasca mostra potencial como terapia para depressão em estudo O ensaio clínico que teve início no Rio Grande do Sul é conduzido pela Fundação Osvaldo Cruz (Fiocruz) em parceria com a GemmaBio, laboratório que a desenvolveu, ligado à Universidade da Pensilvânia (EUA). Parte da contrapartida que o Brasil terá por abrigar o teste é o acesso à terapia por uma fração do preço de mercado (negocia-se menos de 50%). O trabalho que resultou no tratamento dado ao primeiro paciente foi revelado só hoje, mais de um mês depois, pelo Ministério da Saúde em Brasília, durante um evento ligado ao Dia Mundial das Doenças Raras. — O estudo clínico em andamento abre uma frente de ação que pode transformar a vida de famílias e crianças que lidam no dia a dia com a doença — afirmou em discurso o presidente da Fiocruz, Mario Moreira. — O acordo de incorporação de tecnologia também garante a abertura de caminhos para acesso a uma terapia gênica inovadora pela primeira vez no Sistema Único de Saúde. O Brasil se qualificou para realizar o ensaio clínico, em parte, por a Fiocruz já dominar a tecnologia de vetores virais que a terapia usa. A manipulação de vírus para fins terapêuticos era necessária, por exemplo, para as vacinas de Covid-19 que a fundação produziu no período crítico da pandemia. O teste pela qual a terapia está passando agora é de fase 1/2, ou seja, para tanto avaliar segurança e tolerância da terapia quanto buscar indicadores preliminares de eficácia. Nessa etapa são selecionados poucos pacientes. O segundo deve receber o tratamento "nos próximos meses" diz a Fiocruz. No registro do teste clínico, a GemmaBio estima que o tratamento deve ser concedido a 22 crianças no teste. São recrutados bebês entre duas semanas de idade até um ano: período crítico de desenvolvimento em que a terapia tem mais chance de funcionar. O medicamento em teste foi desenvolvido contra a AME de tipo 1, a mais grave. Por privar os músculos de estímulo neural, ela submete as crianças a um declínio progressivo de funções vitais como mastigar, engolir e até respirar. Infecção do bem Para corrigir o gene defeituoso que está na origem dessa degeneração, os pesquisadores inseriram cópias corrigidas do gene em um vírus adeno-associado (AAV), que busca "infectar" o paciente com a cura. A inoculação é feito por meio de uma injeção na estrutura do cérebro chamada cisterna magna, que por meio do fluido cerebrospinal é capaz de levar o medicamento diretamente ao sistema nervoso central. A ideia é que ele atinja mais regiões do cérebro e da medula espinhal, as partes do organismos afetadas pela doença. "Esta via ainda permite administrar o medicamento inclusive em pacientes que tenham anticorpos contra o vírus utilizado na terapia", explica em comunicado Jonas Saute, médico do Hospital de Clínicas envolvido no trabalho. "A equipe médica está monitorando o primeiro paciente, esperando ver o benefício terapêutico e o seu progresso nos marcadores de desenvolvimento neural." O CEO da GemmaBio, James Wilson, divulgou hoje um comunicado sobre o início do ensaio clínico. "Gostaria de expressar nossa gratidão à jovem criança e à sua família, que foram corajosos em ser os primeiros a aceitar nossa terapia gênica experimental contra AME-1", afirmou. "Estamos muito felizes por termos alcançado este marco juntos e somos gratos aos nossos dedicados parceiros da Fiocruz, de Bio-Manguinhos, do Ministério da Saúde, da Anvisa." O teste de fase 1/2 da terapia experimental deve ser concluído até o final de 2028, indica o registro do procedimento nos EUA. Após essa etapa, se o tratamento for bem sucedido, ele se qualifica para um teste de fase 3, que avalia a eficácia com critérios mais rígidos.